突破性研究成果:动物实验验证再生奇迹
引言:严谨验证,铸就信心——从实验室走向临床的坚实桥梁
动物实验是评估新型医疗技术安全性和有效性的关键环节,是连接基础研究与临床应用的不可或缺的桥梁。我们选择新西兰大白兔作为主要的软组织再生研究模型,因其在生理、解剖结构以及对生物材料的反应等方面与人类具有一定的相似性,且易于操作和管理。所有动物实验均严格遵守国际认可的动物福利和实验操作指南(如AAALAC认证标准或等效标准),并获得了机构动物伦理与使用委员会(IACUC)的批准。以下将系统展示我们在兔子缺损模型上取得的各项突破性再生效果。
应用一:可吸收手术缝线——加速创面愈合,优化修复质量
背景挑战:传统手术缝线,尤其是不可吸收缝线,可能在体内引起持续的异物反应、炎症,甚至成为细菌定植的位点,影响伤口愈合质量,导致瘢痕增生或愈合延迟。理想的可吸收缝线应具备良好的生物相容性、足够的初期抗张强度、可预测的吸收时间和对组织修复的积极促进作用。
实验设计:我们建立了兔背部皮肤全层切口模型。将实验动物随机分为两组:实验组采用本可溶性胶原蛋白材料制成的可吸收缝线进行伤口缝合;对照组采用市售常用的可吸收缝线(PGA缝线)。在术后不同时间点(3天、7天、18天)观察并记录创面愈合情况,包括大体外观(红肿、渗出、愈合速度)、组织学评估(炎症细胞浸润程度、新生血管密度、胶原沉积与重塑情况、表皮再生完整性)以及创面抗张强度等。
核心发现与数据:实验结果显示,与对照组相比,采用本胶原蛋白缝线的实验组创面愈合速度更快,早期炎症反应显著减轻。组织学检查发现,实验组创面有更早的新生血管形成和更有序的胶原纤维沉积,表皮再生更为完整,瘢痕形成程度较低。例如,一项专利数据显示,特定工艺制备的獭狸胶原蛋白缝线在体外降解实验中表现出良好的强度维持和降解特性 (CN105148318A - 一种獭狸医用可吸收胶原蛋白缝合线的制备方法)。我们的材料也表现出类似的优异性能,具体数据已在我们的bioRxiv预印本中详细呈现-https://doi.org/10.1101/2025.05.19.25325989
结论意义:本可溶性胶原蛋白基手术缝线能显著加速伤口愈合速率,减轻炎症反应,促进高质量的皮肤再生(可能减少瘢痕形成,改善外观和功能)。其优异的生物相容性和可控的降解特性,使其在各类外科手术中,特别是在对愈合质量有较高要求的领域(如整形外科、显微外科),具有巨大的临床应用潜力。
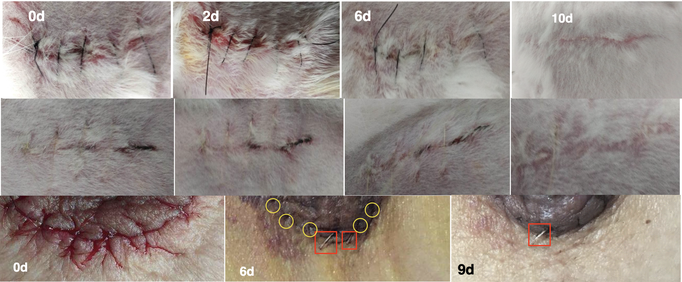
图ー 第1排:兔子背部皮肤伤口用黑色缝线缝合。第2排:兔子背部皮肤上的透明缝线。第3排:患者胸部皮肤伤口用透明缝线缝合。
伤口愈合效果均良好。
应用二:再生型人工肌腱——世界首次!成功攻克大面积肌腱缺损修复难题
背景挑战:大面积肌腱缺损,常见于严重的运动创伤、交通事故或肿瘤切除术后,是临床骨科和运动医学领域公认的重大难题。现有治疗手段,如自体肌腱移植(受限于供区选择和损伤、移植物长度有限)、异体肌腱移植(存在免疫排斥、疾病传播风险和力学性能下降问题)以及合成材料(生物相容性差、易发生磨损和断裂、无法实现真正的生物学整合),均存在明显局限性,往往导致功能恢复不理想,患者生活质量严重受损。
实验设计:我们建立了兔跟腱(Achilles tendon)大段缺损模型(缺损长度通常超过1.5-2cm,足以被认为是难以自行愈合的“大面积缺损”)。将实验动物随机分组,实验组在缺损处植入本仿生材料构建的组织工程化人工肌腱;对照组可设置为空白缺损不修复组、自体肌腱移植组或市售肌腱修复材料组。在术后不同时间点(通常为4周、8周、12周,部分实验可能延长至24周或更长)通过大体观察、组织学与免疫组化分析以及生物力学测试,全面评估再生肌腱的形态、结构、细胞成分、胶原纤维排列、血管化程度、与骨附着点愈合情况以及最重要的——力学性能恢复和动物肢体功能改善情况。
核心发现与数据:我们自豪地宣布,本研究在世界上首次成功实现了兔大面积肌腱缺损的功能性再生! 植入本仿生人工肌腱后,观察到缺损区域逐渐被新生组织填充,该组织在形态和结构上逐步接近正常肌腱。组织学分析显示,新生组织中富含定向排列的I型胶原纤维和梭形的腱细胞样细胞,并伴有良好的血管化。至关重要的是,生物力学测试结果表明,再生肌腱的抗拉强度、弹性模量等关键力学指标随时间推移显著提升,在实验后期(20周)已接近甚至达到正常肌腱的水平。具体参考我们的预印本数据-https://doi.org/10.1101/2025.05.30.655895
结论意义:本仿生再生材料在肌腱再生领域取得了历史性的、世界级的突破。它首次证明了通过组织工程手段可以有效修复并功能性再生以往被认为难以治愈的大面积肌腱缺损,为运动损伤、退行性肌腱病以及其他原因导致的严重肌腱损伤患者提供了一种全新的、革命性的治疗策略,具有极其重大的临床意义和广阔的市场前景。

图2 a、b、c:人工肌腱移植;d、d1、d2:具有白色外层的20周再生肌腱;d2:已经分离的白色外层。e、e1、e2:20周再生肌腱从中横切一半;e:含尼龙缝线和胶原仿生材料纤维的再生肌腱;e1:横截面;e2:含尼龙缝线但不含仿生胶原纤维的再生肌腱;绿色箭头:再生肌腱;白色箭头:自体肌腱。
应用三:功能性人工肌肉——世界首次!有效应对体积性肌肉损失(VML)挑战
背景挑战:体积性肌肉损失(Volumetric Muscle Loss, VML)是指由于严重创伤(如爆炸伤、车祸)、肿瘤切除或某些先天性疾病导致的大块骨骼肌组织的永久性缺失。VML常导致肢体严重的功能障碍、畸形和生活质量下降。目前,临床上对于VML缺乏有效的修复手段,自体肌肉移植受限于供区大小和功能损失,而现有生物材料往往难以支持大块、有血管和神经支配的功能性肌肉组织的再生。
实验设计:我们在兔特定部位(腹壁)建立了标准化的VML模型(切除腹壁肌肉层 3x3 cm)。实验组在VML缺损区植入本可溶性胶原蛋白基仿生材料构建的肌肉支架(可预先负载促血管生成和促神经再生的生长因子,或与自体干细胞复合)。对照组植入PP(polypropylene)类型支架材料组。评价指标包括:评价指标包括:术后不同时间点(如4周、8周、16周,24周,32周)再生肌肉的体积、重量、与周围健康肌肉的整合情况;组织学 上新生肌纤维的密度、直径、成熟度、毛细血管网络密度;最重要的,通过离体肌肉强度测定,评估再生肌肉的功能恢复程度
核心发现与数据:本研究同样取得了世界首次的重大突破:我们成功实现了兔VML模型中大块功能性骨骼肌的再生!植入本材料支架后,VML缺损区域逐渐被新生肌肉组织填充,其颜色和质地与周围健康肌肉相似。组织学分析证实,新生组织中包含大量排列有序新生肌纤维,并伴有丰富毛细血管网络。结果令人鼓舞:与对照组相比,实验组再生肌肉强度显著恢复,我们bioRxiv预印本数据详细。https://doi.org/10.1101/2025.06.07.657281
结论意义:本技术在VML再生领域实现了里程碑式的进展。它首次有力地证明了,通过先进的仿生组织工程策略,可以有效再生大块的、具有血管化、神经支配和收缩功能的骨骼肌组织。这为因创伤、肿瘤等原因导致VML的患者带来了前所未有的功能重建希望,有望从根本上改变VML的治疗格局。
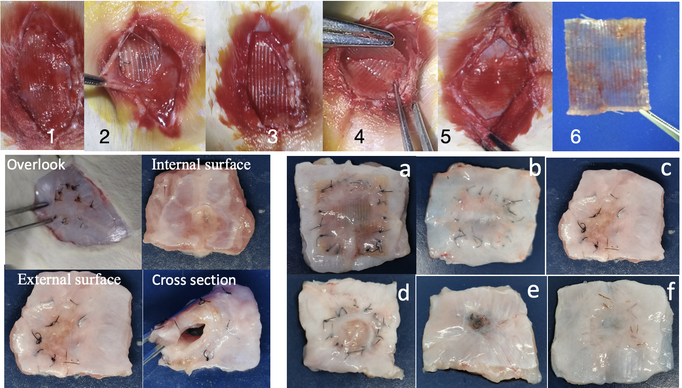
图3:疝气贴片移植和腹壁再生:最上排:移植术后17天的疝气贴片 in vivo,左下图板:16周的再生腹壁。右下图板:按时间顺序再生的腹壁(尼龙缝线4、8、16、24、32周);f:胶原缝合线-32周)。
应用四:引导性人工神经——促进神经修复,恢复组织功能
背景挑战:周围神经长段缺损(通常指缺损长度>1-2cm)的修复是神经外科面临的经典难题。自体神经移植虽被视为“金标准”,但存在供区神经功能丧失、来源有限、神经直径不匹配等问题。人工神经导管(Nerve Guidance Conduits, NGCs)作为一种替代方案,其性能仍有较大提升空间,尤其是在促进长距离轴突再生、提高再生神经功能恢复质量方面。
实验设计:我们建立了兔坐骨神经(一种主要的混合性周围神经)20mm的长段缺损模型。实验组采用本可溶性胶原蛋白材料制成的人工神经导管桥接神经断端。在术后不同时间点(如4周、8周、12周,24周,36周)进行综合评估,包括:再生神经束的大体形态和组织学结构(如轴突数量、直径、髓鞘厚度、施万细胞活性)。
核心发现与数据:实验结果表明,本材料构建的人工神经导管能够有效引导和支持轴突跨越长距离缺损再生。组织学观察显示,导管内形成了包含大量有髓和无髓神经纤维的再生神经束,施万细胞增生活跃,表明髓鞘形成正常。组织学分析进一步证实了再生轴突和髓鞘的结构。尽管在某些组织学指标上可能略逊于自体移植,但功能恢复良好,具体数据见bioRxiv预印本。https://doi.org/10.1101/2025.06.19.660623
结论意义:本可溶性胶原蛋白基人工神经导管为周围神经长段缺损的修复提供了一种极具前景的新型生物材料。它能够有效引导轴突再生,促进髓鞘形成,并最终恢复神经传导功能和靶器官功能。相较于自体神经移植,它避免了供区损伤和来源限制;相较于部分现有神经导管,它可能在促进功能性恢复方面展现出更优的性能。

图4 再生神经。按时间序列排列的再生神经 (8, 12, 24, 36 weeks);autologous: 兔子自体坐骨神经。
研究成果总结与科学价值
共性优势提炼:上述各项动物实验结果共同证明了我们的可溶性胶原蛋白基仿生再生材料具有优异的生物相容性(植入后无明显不良反应)、强大的组织再生诱导能力(能够主动引导多种类型细胞的行为)和显著的修复效果(在结构和功能上均接近正常组织)。
科学意义:这些“世界首次”的成果不仅验证了材料本身的优越性,也为深入理解特定软组织(如肌腱、肌肉)的复杂再生机制提供了新的视角和研究工具。它们挑战了传统观念中某些组织(如大块肌肉)难以通过组织工程方法实现功能性再生的局限。
临床转化潜力:基于在兔模型上获得的坚实、积极的动物实验数据,我们对本材料未来在人体多种软组织缺损修复中的临床应用抱有极大信心。这些成果为后续的临床前研究和临床试验设计奠定了坚实的基础。
统一链接:我们诚邀您查阅我们在 bioRxiv 平台上发表的相关预印本,以获取更详细的实验数据和方法学描述:
- [预印本标题1:关于肌腱再生的研究] - [bioRxiv链接]https://doi.org/10.1101/2025.05.30.655895
- [预印本标题2:关于VML再生的研究] - [bioRxiv链接]https://doi.org/10.1101/2025.06.07.657281
- [预印本标题3:关于神经再生的研究] - [bioRxiv链接]https://doi.org/10.1101/2025.06.19.660623
- [预印本标题4:关于手术缝线的研究] - [bioRxiv链接] https://doi.org/10.1101/2025.05.19.25325989
重塑多个医疗领域的未来, 创新材料赋能多元再生
我们的可溶性胶原蛋白基仿生再生材料,凭借其独特的核心成分、精妙的仿生设计理念及在关键动物实验中已证实的卓越再生能力,并不仅仅是针对单一临床问题的解决方案。它本质上是一种具有广泛适用性的平台型再生医学技术。通过对材料的微观结构、宏观形态、力学性能以及所负载的生物活性因子进行精密调控和定制化设计,我们有能力将其拓展应用于更多种类、更复杂场景的软组织缺损修复,从而重塑多个医疗领域的未来。
已验证应用的临床深化与市场拓展 基于已取得的突破性动物实验成果,我们首先致力于在以下领域进行临床深化和市场拓展:
- 高端可吸收手术缝线市场:针对整形外科、显微外科、心血管外科、神经外科等对缝合材料的生物相容性、抗炎性、促愈合能力以及低瘢痕形成有极高要求的科室,开发具有更优异性能的特种缝线产品。
- 肌腱/韧带修复的广泛适应症:除了急性创伤导致的肌腱/韧带断裂(如肩袖撕裂、跟腱断裂、交叉韧带损伤),还将积极探索其在治疗慢性劳损(如网球肘、跟腱炎)、退行性病变以及先天性肌腱/韧带发育不良等疾病中的应用,覆盖运动医学、骨科、康复医学及老年医学等广阔市场。
- VML治疗的多元化场景:除了因创伤和肿瘤切除导致的VML,我们还将探索本技术在治疗某些先天性肌肉发育不良、肌营养不良症(作为辅助治疗或细胞治疗的载体)、以及因长期废用或神经损伤导致的肌肉萎缩等复杂情况下的应用潜力。
- 神经修复的精细化与复杂化应用:针对不同直径(从细小的指神经到较粗的臂丛神经)、不同类型(感觉神经、运动神经、混合神经)以及不同长度的神经缺损,开发系列化的人工神经导管产品。同时,探索其在神经移植(如神经束桥接)、神经瘤预防以及中枢神经系统损伤修复(作为细胞或药物递送载体)等更复杂场景中的应用。
未来重点拓展的全新应用领域
凭借本材料平台的强大延展性,我们正积极规划并开展以下全新应用领域的前期研究:
1. 人工小口径血管 (<6mm)——攻克心血管“最后一公里”
临床痛点:冠状动脉搭桥术、外周血管疾病(如下肢动脉闭塞)、血液透析用动静脉内瘘的建立等,均对直径小于6毫米的人工血管(Small-Diameter Vascular Grafts, SDG)存在巨大且迫切的需求。然而,目前临床上广泛使用的合成材料(如ePTFE, PET)SDG,在应用于小口径场景时,普遍面临内膜增生、血栓形成、顺应性不匹配、长期通畅率低等难题,远未达到理想效果。自体血管(如大隐静脉、桡动脉)移植虽效果较好,但来源有限,且会造成供区损伤。
本材料的潜力:可溶性胶原蛋白具有天然的低致血栓性和促进内皮细胞粘附、增殖与功能化的优良特性。通过静电纺丝、3D生物打印等技术,我们可以构建出具有仿生多层结构(模拟血管内膜、中膜、外膜)、可控孔隙率和与天然血管相匹配的力学顺应性的小口径管状支架。该支架有望快速实现内皮化,抑制平滑肌细胞过度增生,从而显著提高长期通畅率,并具备良好的生物降解和组织重塑能力。
预期效益:为数以百万计的心血管疾病患者提供一种优于现有自体血管移植和合成材料SDG的解决方案,显著降低手术风险、减少再狭窄和血栓并发症,改善患者远期预后。
市场规模预估:全球心血管疾病治疗市场巨大,仅冠脉搭桥手术每年即达数百万例。小口径人工血管市场预计将以超过10%的年复合增长率持续增长。
2. 组织工程化气管/支气管——重获顺畅呼吸的希望
临床痛点:长段气道狭窄(如结核、创伤、医源性损伤导致)、气管/支气管肿瘤切除后的大段缺损、以及某些先天性气管畸形(如气管软化症、先天性气管狭窄),目前缺乏理想的修复或替代材料。自体组织修复(如带蒂肌皮瓣、肋软骨移植)技术复杂、创伤大、并发症多。同种异体气管移植则面临免疫排斥和供体来源极其匮乏的困境。
本材料的潜力:利用本可溶性胶原蛋白材料,结合生物3D打印或模具成型技术,我们可以构建出具有一定径向支撑强度(可复合PCL等增强材料或通过特殊结构设计实现)和良好生物相容性的管状支架。该支架可设计为双层或多层结构,分别引导气道上皮细胞和软骨细胞的再生与分化,最终形成具有正常生理功能(如黏液纤毛清除、气体交换辅助、保持管腔通畅)的组织工程化气管/支气管。
预期效益:为复杂气道疾病患者提供一种潜在的根治性治疗手段,避免气管切开长期带管的痛苦,显著改善呼吸功能和生活质量。
市场规模预估:虽然相对小众,但临床需求迫切,属于典型的“未被满足的医疗需求”领域,具有重要的社会价值和人道主义意义。
3. 再生型人工食管——恢复尊严“食”光
临床痛点:食管癌是我国高发恶性肿瘤之一,食管切除术是主要的治疗手段,术后常需进行食管重建。目前常用的重建方式如胃代食管、结肠代食管或空肠代食管,均存在手术复杂、创伤大、吻合口瘘、反流性食管炎、狭窄、以及长期生活质量(如进食、消化功能)受影响等问题。化学烧伤、意外创伤或某些先天性疾病(如先天性食管闭锁)也可能导致食管大段缺损,修复极为困难。
本材料的潜力:通过构建具有仿生多层结构(模拟食管黏膜层、黏膜下层、肌层)的管状胶原支架,并可选择性负载促进上皮细胞和肌细胞再生的生长因子,有望引导宿主细胞原位再生出具有正常蠕动功能和屏障功能的食管组织。这种“原位再生”的人工食管,理论上能更好地恢复食管的生理功能,减少并发症。
预期效益:为食管缺损患者提供一种创伤更小、并发症更少、术后生活质量更高、更接近生理状态的食管重建新方案,显著改善患者的营养状况和生存尊严。
市场规模预估:食管癌发病率较高,对高质量食管重建技术的需求持续存在。该领域的技术突破将带来巨大的临床价值。
4.作为细胞培养基材的应用(代替温度敏感性材料PIPAAM/PNIPAAM)
临床痛点:人工合成温度敏感型高分子材料(PNIPAAm和PIPAAm)可以避免酶对细胞的损伤,因此广泛应用于培养细胞片。但是,其化学成分、三维结构和物理性质与生物体内的天然微环境明显不同。对干细胞的影响尤为重要:干细胞对微环境感知非常敏感,培养基质的物理化学特性直接影响自我更新能力和分化潜能。根据研究,PNIPAA合成材料的表面缺乏天然ECM可以提供的复杂生物信号(特定的配体、生长因子结合部位、适当的刚度等),干细胞的分化方向意外偏离,长期的“干”状态难以维持,影响再生治疗的最终效果。
胶原蛋白片的优越性:医疗级的可溶性胶原蛋白片具有无与伦比的生物相容性,免疫原性非常低,具有营养性,促进细胞的附着、扩散、移动和增殖。三维网络结构为细胞提供了良好的生长微小环境。其分解产物小分子肽和氨基酸,可以由身体重复使用。避免残留异物。直接移植胶原蛋白培养细胞,免除冷却剥离操作。这具有革命性的优势,细胞片不仅是细胞层,也是生物活性基质的“复合物”。避免剥落,简化过程,节省时间和人手,避免剥落对细胞的损伤和生理压力,细胞更好地维持原来的表型特性、蛋白质表达光谱和特定的生物功能,移植后的细胞在发挥治疗效果方面非常重要。对敏感的干细胞有更深的影响。胶原蛋白基质比玻璃和塑料基质更能促进细胞的粘附、增殖、分化的报道也很多(使用新田明胶原蛋白的细胞培养法)。
关键要点总结
通过在兔缺损模型上的系列严格动物实验,我们成功验证了可溶性胶原蛋白基仿生再生材料在手术缝线、人工肌腱、人工肌肉(VML)和人工神经等多个应用方向上的卓越再生效果。其中,肌腱大缺损和VML的功能性再生更是取得了世界首次的突破性进展,充分展示了本技术的先进性、有效性和巨大的临床转化潜力。
产品蓝图:高强度胶原蛋白医学再生材料的植入类产品矩阵
基于高强度可溶性胶原蛋白医学再生材料的卓越特性,其在植入类医疗器械领域具有广阔的开发前景。这些潜在产品可以根据材料的加工形态或目标应用的组织器官进行分类,以下将详细阐述其可能的产品矩阵。
1. 按材料形态划分的产品可能性
材料的形态直接决定了其在临床上的应用方式和场景。高强度胶原蛋白材料优异的可加工性使其能够被制成多种形态的产品:
膜/片剂型产品 (Membrane/Sheet Forms)
应用领域:主要用于组织的覆盖、屏障保护、引导组织再生、缺损修补以及作为细胞或药物的承载体。
具体产品示例:
-
通用外科/多科室:
- 疝修补片:用于腹股沟疝、切口疝、脐疝等的无张力修复。
- 皮肤修复膜/人工真皮:用于烧烫伤、慢性溃疡、皮肤缺损的覆盖与再生。研究表明胶原蛋白是ECM的重要组成成分,在创面愈合的每个阶段都有重要作用 (PMC11630175)。
- 可吸收防粘连膜:用于手术后防止组织间粘连,尤其在腹盆腔手术和肌腱手术中。
-
神经外科:
- 硬脑膜/脊膜补片:用于神经外科手术后硬脑(脊)膜的缺损修复,防止脑脊液漏。胶原蛋白敷料已用于神经外科修复 (高·见|重组胶原蛋白)。
-
心胸外科:
- 心包补片:用于心脏手术后心包缺损的修复或重建。
-
口腔科:
- 口腔修复膜:用于口腔黏膜缺损修复。
- 引导组织再生(GTR)膜/引导骨再生(GBR)膜:用于牙周炎治疗中引导牙周组织再生或牙槽骨增量术中引导新骨形成。利用重组人Ⅰ型胶原蛋白制成的胶原膜展现出强大的抗酶解能力和屏障稳定性 (PMC11879737)。
-
妇产科/泌尿科:
- 盆底重建修补片:用于压力性尿失禁、盆腔器官脱垂的修复。
- 阴道壁/尿道壁修复片:用于修复相关组织的缺损或狭窄。
- 膀胱扩大或修复片:用于小膀胱扩大成形术或膀胱损伤修复。
-
普外科/消化外科:
- 肛瘘修补片/塞:用于复杂性肛瘘的治疗。
- 肠壁/胃壁修复加强片:用于吻合口加固或穿孔修补。
-
整形外科/美容科:
- 乳房植入物包膜挛缩预防/修复补片。
- 面部轮廓填充支撑材料:作为软组织填充剂的支撑结构。
-
眼科:
- 角膜修复材料:作为角膜基质替代物或药物缓释载体。重组人胶原蛋白已被用于角膜修复研究 (PMC11879737)。
- 巩膜扣带术辅助材料/眼眶植入物包裹材料。
-
耳鼻喉科:
- 鼓膜修复片:用于鼓膜穿孔的修复。
- 鼻中隔修复片:用于鼻中隔穿孔修复或鼻整形支撑。
-
骨科:
- 关节软骨修复膜/片:引导软骨细胞再生,修复关节软骨缺损。EDC/NHS交联重组I型胶原水凝胶已成功修复骨关节软骨 (中国医疗器械杂志PDF)。
- 骨缺损覆盖膜:用于引导骨再生,防止软组织长入。
线型产品 (Suture/Fiber Forms)
应用领域:主要用于组织的缝合、捆扎,或作为编织复杂结构的基础材料,构建具有特定取向性的纤维网络。
具体产品示例:
-
各手术科室:
- 新型可吸收手术缝合线:这是用户团队已取得优良结果的核心产品之一,具有低炎症反应、微小疤痕形成和促进愈合的特性,有望替代或优于现有多种可吸收缝线。
-
骨科/运动医学:
- 人工肌腱/韧带的核心编织材料:利用高强度胶原蛋白线编织成具有仿生结构和力学性能的人工肌腱或韧带。
- 加强缝合线:用于肌腱、韧带等高张力组织的修复缝合。
-
组织工程:
- 取向性纤维支架:利用胶原蛋白细丝通过静电纺丝或微加工技术构建具有特定微观结构的支架,用于引导细胞取向生长(如神经、肌肉细胞)。
管型产品 (Tubular Forms)
应用领域:主要用于引导中空管道组织(如神经、血管、尿道等)的再生,作为临时或永久的管道替代物,或作为药物/细胞输送的通道。
具体产品示例:
-
神经外科/手外科:
- 人工神经导管:用于周围神经缺损的桥接修复,引导轴突再生。用户团队已在兔子坐骨神经缺损修复中取得成功。
-
心血管外科:
- 小口径人工血管 (直径<6mm):这是目前人工血管领域的一大挑战,高强度、低免疫原性的胶原蛋白管有望在该领域取得突破,用于冠状动脉搭桥、外周血管重建等。重组人胶原蛋白涂层已显示出优异的抗血栓特性 (PMC11879737)。
- 血管支架的生物可吸收涂层或基材:用于改善支架的生物相容性,或作为全降解支架的材料。
-
泌尿外科:
- 人工输尿管/人工尿道:用于修复因创伤、肿瘤或先天性疾病导致的输尿管/尿道缺损或狭窄。
-
消化外科/肝胆外科/呼吸科:
- 人工胆管/人工食管/人工气管:作为内衬材料或部分替代物,用于修复相关管道的缺损或狭窄。聚酯纤维(涤纶)常用于大中口径血管替换,但小口径合成血管仍面临挑战
海绵/凝胶/颗粒状产品 (Sponge/Hydrogel/Granule Forms)
应用领域:主要用于快速止血、填充不规则组织缺损、作为组织工程支架、或作为药物/细胞的缓释载体。
具体产品示例:
-
各手术科室:
- 高效生物可吸收止血海绵/粉末:利用胶原蛋白的天然止血特性 (PMC11630175),制成快速起效且可完全吸收的止血材料。
-
骨科/口腔科:
- 骨缺损填充颗粒/凝胶:用于填充骨囊肿、拔牙窝或骨折不愈合等造成的骨缺损,可复合骨生长因子或自体骨髓。胶原蛋白已被广泛应用于骨修复材料 (中国组织工程研究)。
- 可注射骨修复材料:通过微创方式将胶原基材料注入骨缺损部位。
-
组织工程/再生医学:
- 多孔海绵状支架:用于填充不规则形状的组织缺损,如用户团队在兔子腹壁肌肉缺损修复中应用的片状/海绵状材料。
- 可注射水凝胶:用于微创治疗,如软骨修复、心肌修复或细胞递送。重组胶原水凝胶在糖尿病足溃疡修复中显示出良好效果 (中国医疗器械杂志PDF)。
-
药物释放系统:
- 缓释载体:利用胶原蛋白的凝胶或多孔结构,负载抗生素、生长因子、抗肿瘤药物等,实现局部、持续的药物释放。
编织/复杂三维结构产品 (Woven/Complex 3D Constructs)
应用领域:主要用于模拟具有复杂三维结构和特定力学性能的组织或器官,或用于个性化定制的植入物。
具体产品示例:
-
骨科/运动医学:
- 编织型人工肌腱/韧带:通过精确控制胶原蛋白线的编织方式,模拟天然肌腱/韧带的纤维束结构和力学特性。用户团队在兔子跟腱修复中的成功是重要基础。
-
组织工程:
- 3D打印/生物编织的定制化组织/器官支架:这是组织工程领域的前沿方向。利用高强度胶原蛋白作为“生物墨水”或编织材料,结合3D打印或生物编织技术,有望构建出具有特定形态和内部结构的支架,用于修复或替换更复杂的组织,如血管、食管、气管、胆管、人工尿道、输尿管,甚至大肠小肠等结构的早期探索。
-
心血管外科:
- 编织型心脏瓣膜框架/瓣叶:探索用于心脏瓣膜修复或替换的全生物材料方案。
- 编织型大血管补片:用于修复主动脉等大血管的缺损。
2. 按目标应用组织/器官划分的产品可能性
从临床需求和人体系统角度出发,高强度胶原蛋白材料的潜在产品可归纳如下,这与按形态分类存在交叉,但更侧重于应用场景:
神经系统修复与再生产品
- 核心产品:人工神经导管 (管型)、硬脑膜/脊膜补片 (膜/片状)、神经修复凝胶/支架 (凝胶/海绵状)。
- 临床潜力:解决神经断裂、缺损(尤其是存在间隙的缺损)后的功能恢复难题,降低神经瘤形成风险,改善患者预后。用户在坐骨神经缺损修复中的成功案例为此方向提供了关键的实验证据。
运动系统 (肌肉、肌腱、韧带、骨、软骨) 修复与再生产品
- 核心产品:人工肌腱/韧带 (线型、编织型)、肌肉修复片/支架 (片状、海绵状、编织型)、骨修复材料 (膜、颗粒、海绵、3D打印支架)、软骨修复膜/支架 (膜/片状、凝胶状)。
- 临床潜力:广泛应用于运动损伤(如韧带撕裂、跟腱断裂)、退行性病变(如骨关节炎)、创伤或肿瘤切除导致的骨骼肌肉系统组织缺损,旨在实现结构与功能的双重重建。用户在兔子跟腱和腹壁肌肉缺损修复中的成功案例是此领域的有力证明。重组人胶原蛋白已被广泛用于皮肤、骨、软骨、肌腱和韧带等多种组织的修复和再生 (PMC11879737)。
心血管系统修复与再生产品
- 核心产品:心包补片 (膜/片状)、小口径人工血管 (管型、编织型)、血管内支架的生物可吸收涂层或基材、心脏瓣膜修复/替换材料 (编织/膜片复合结构)。
- 临床潜力:针对血管狭窄/闭塞、瓣膜病变、心肌损伤等重大心血管疾病的治疗需求。材料的低免疫原性、抗血栓形成潜力(通过表面修饰或特定胶原类型选择)以及促进内皮化的能力是其在该领域应用的关键。重组人Ⅰ型和Ⅲ型胶原蛋白能够恢复心肌梗死后的心肌机械性能并抑制病理重塑 (PMC11879737)。
皮肤及其他软组织修复与再生产品
- 核心产品:皮肤修复膜/人工真皮 (膜/片状)、可吸收手术缝线 (线型)、创面愈合敷料/凝胶 (膜/片、凝胶、海绵状)、疝修补片 (膜/片、编织型)、乳房重建补片 (膜/片状)。
- 临床潜力:广泛应用于各类皮肤缺损(烧烫伤、慢性创面)、创伤修复、整形美容领域,旨在实现功能恢复与美学效果的统一。胶原蛋白敷料在皮肤科、口腔科等领域应用广泛 (高·见|重组胶原蛋白)。
消化系统管道及实质器官修复与再生产品
- 核心产品:肠壁/胃壁修复加强片 (膜/片状)、食管/气管/胆管支架或内衬 (管型、编织型)、肛瘘修补塞/片 (海绵/片状)。
- 临床潜力:针对吻合口瘘、消化道穿孔、良恶性狭窄等消化系统疾病,提供新的修复方案,改善患者生活质量。
泌尿生殖系统修复与再生产品
- 核心产品:人工尿道/输尿管 (管型)、膀胱壁修复/扩大片 (膜/片状)、盆底重建修补片 (膜/片、编织型)、阴道壁修复材料 (膜/片状)。
- 临床潜力:解决因先天畸形、创伤、肿瘤切除或衰老等导致的泌尿生殖系统结构和功能障碍,如尿道狭窄、膀胱容量不足、盆腔器官脱垂等。胶原蛋白在妇产科领域展现出巨大应用潜力,用于组织重建及填充 (汉斯出版社)。
五官科 (眼、耳、鼻、喉、口腔) 精细修复与再生产品
- 核心产品:口腔修复膜/GBR/GTR膜 (膜/片状)、鼓膜修复片 (膜/片状)、眼科植入物 (如角膜基质替代材料、巩膜加强材料)、鼻中隔/耳廓软骨修复支架 (3D打印/膜片)。
- 临床潜力:五官科组织结构精细复杂,功能要求高。高强度胶原蛋白材料的优异生物相容性和可塑性,使其在这些精细结构的修复和功能重建方面具有独特优势。
这一庞大的产品矩阵充分展示了高强度可溶性胶原蛋白医学再生材料作为一种平台型技术的巨大潜力。通过不同的加工工艺和与其他生物活性物质的复合,有望开发出一系列针对特定临床需求的创新医疗器械产品。
掘金蓝海:重点植入类产品的市场价值评估与替代潜力
高强度可溶性胶原蛋白医学再生材料凭借其卓越性能,有望在多个植入类医疗器械细分市场中占据重要地位。以下将对部分重点产品的全球市场价值进行评估,并分析其相对于传统材料的市场替代潜力。需要强调的是,此处提供的数据和分析主要基于现有公开信息和合理的行业逻辑推演。
全球医用植入物市场规模庞大且持续增长。根据 Custom Market Insights (CMI) 的数据,2023年全球医用植入物市场规模已达到1126亿美元,预计到2032年将增长至2036亿美元,年复合增长率(CAGR)为6.8%。另有报告指出,2023年市场规模为1102.5亿美元,预计到2033年达到2147.6亿美元,CAGR为6.90% (GlobeNewswire)。这些数据为我们评估细分市场潜力提供了宏观背景。
产品/产品类别:可吸收手术缝线 (Absorbable Surgical Sutures
- 核心功能与应用场景:用于体内各类组织的缝合、结扎,在伤口愈合后可被人体吸收,无需二次手术拆线。广泛应用于普外科、妇产科、骨科、神经外科、整形外科、眼科、口腔科等几乎所有手术科室。解决的关键问题是避免异物残留、减少组织反应和感染风险、提升患者舒适度。
- 适用材料形态:单股或多股编织线型。
- 目标临床应用领域:各类手术中的软组织缝合,特别适用于对疤痕形成和炎症反应有较高要求的精细手术和儿童手术。
-
全球市场规模评估 (年度):
- 当前市场总值:全球手术缝线市场是一个数十亿美元级别的市场,其中可吸收缝线占据重要份额。根据推算,全球可吸收手术缝线市场规模预估约为40-60亿美元 (数据年份:2023-2024年,此为基于整体手术量和缝线使用情况的行业估算,具体数据需查阅专项报告)。
- 估算方法/数据来源:行业综合估算。
-
主要区域市场分布 (年度):
- 北美市场:约 35-40%
- 欧洲市场:约 25-30%
- 亚太市场:约 20-25% (增长最快)
- 其他区域:约 10-15%
-
与现有传统产品的对比及替代潜力:
- 主要竞品/传统方案:天然可吸收缝线 (羊肠线、传统胶原线),合成可吸收缝线 (PGA, PGLA, PDO, PGCL等)。
- 本材料产品的核心优势:极低的免疫原性与炎症反应(优于羊肠线和部分合成线),优异的生物相容性与组织整合,促进伤口愈合与减少疤痕形成(用户初步结果支持),理想的力学性能(高强度)与操控性。
- 预期市场替代潜力评估:高。尤其在高端市场,如整形美容、儿童外科、眼科等对缝线性能要求极高的领域。
- 替代可行性分析:若临床能证实其在安全性(低炎症、低过敏)、有效性(愈合质量、抗张强度维持)和成本效益上优于或持平于高端合成可吸收缝线,市场替代潜力巨大。
- 本材料在该产品的年度商业价值潜力估算:若能占据全球可吸收缝线市场5-15%的份额,则年度商业价值可达2亿至9亿美元。
产品/产品类别:疝修补片 (Hernia Repair Mesh/Patch)
- 核心功能与应用场景:用于腹股沟疝、切口疝、脐疝等腹壁缺损的无张力修复,通过加强腹壁组织,防止疝内容物突出。是普外科最常用的植入物之一。
- 适用材料形态:膜/片状,可为编织或非编织结构。
- 目标临床应用领域:普外科的各类疝修补手术。
-
全球市场规模评估 (年度):
- 当前市场总值:全球疝修补装置(包括补片)市场规模约为50-70亿美元 (数据年份:2023-2024年,行业估算)。其中,生物补片和可吸收补片是增长较快的细分市场。
- 估算方法/数据来源:行业综合估算。
- 主要区域市场分布 (年度):与缝线市场类似,北美、欧洲占比较高,亚太增长快。
-
与现有传统产品的对比及替代潜力:
- 主要竞品/传统方案:不可吸收合成补片 (聚丙烯PP、聚酯PET、ePTFE),部分可吸收合成补片,生物补片 (脱细胞异体/异种真皮ADM/SIS)。
- 本材料产品的核心优势:优异的生物相容性与低慢性炎症/异物反应(对比PP补片),引导宿主组织再生与血管化,完全可吸收并被自体组织替代,足够的初期强度与良好的柔韧性。
- 预期市场替代潜力评估:高。尤其对于追求更高生活质量、关注远期并发症的患者,以及在污染或潜在污染环境下的手术。有望替代部分合成补片和现有生物补片(ADM/SIS等可能存在免疫原性和成本问题)。
- 替代可行性分析:临床证据需证明其在复发率、慢性疼痛、感染率等方面优于或不劣于现有金标准产品,同时具备良好的操控性和成本效益。
- 本材料在该产品的年度商业价值潜力估算:若能占据全球疝修补补片市场(特别是生物补片和高端合成补片领域)10-20%的份额,则年度商业价值可达5亿至14亿美元。
产品/产品类别:人工神经导管 (Nerve Guidance Conduit / Nerve Tube)
- 核心功能与应用场景:用于周围神经缺损的桥接修复,为断裂的神经两端提供一个引导再生的通道,促进轴突生长和功能恢复。
- 适用材料形态:管型。
- 目标临床应用领域:神经外科、手外科、骨科、创伤外科等涉及周围神经损伤修复的领域。
-
全球市场规模评估 (年度):
- 当前市场总值:全球神经修复与再生市场中,人工神经导管是一个快速增长的细分领域,市场规模预估为3-5亿美元 (数据年份:2023-2024年,行业估算)。
- 估算方法/数据来源:行业综合估算。
- 主要区域市场分布 (年度):北美和欧洲技术领先,市场份额较大。
-
与现有传统产品的对比及替代潜力:
- 主要竞品/传统方案:自体神经移植 (金标准但供区损伤、数量有限),脱细胞神经移植物 (异体/异种),其他合成/天然材料导管 (PGA、壳聚糖、硅胶管等)。
- 本材料产品的核心优势:卓越的生物相容性与低免疫原性,促进神经轴突生长和髓鞘形成(用户坐骨神经修复成功是强力证明),可控的降解速率,良好的半透性和机械性能。
- 预期市场替代潜力评估:高。尤其对于中小段神经缺损,有望成为自体神经移植的重要替代方案,并优于现有部分人工导管。
- 替代可行性分析:临床试验需证明其在神经再生速度、功能恢复程度、感觉和运动恢复质量上接近或优于自体移植,且操作简便。
- 本材料在该产品的年度商业价值潜力估算:若能占据人工神经导管市场15-30%的份额,并部分替代自体移植,则年度商业价值可达0.45亿至1.5亿美元。
产品/产品类别:皮肤修复膜/人工真皮 (Skin Repair Membrane / Dermal Substitute)
- 核心功能与应用场景:用于治疗大面积烧烫伤、慢性难愈性创面(如糖尿病足、压疮)、皮肤撕脱伤、肿瘤切除后皮肤缺损等,提供临时或永久的皮肤覆盖,促进创面愈合,减少感染,改善外观。
- 适用材料形态:膜/片状,可为多孔结构。
- 目标临床应用领域:烧伤科、整形外科、皮肤科、创面治疗中心。
-
全球市场规模评估 (年度):
- 当前市场总值:全球先进伤口护理市场巨大,其中皮肤替代品/生物敷料市场规模约为25-35亿美元 (数据年份:2023-2024年,行业估算)。重组胶原蛋白在创面修复敷料中应用广泛 (2024重组胶原蛋白行业白皮书)。
- 估算方法/数据来源:行业综合估算。
- 主要区域市场分布 (年度):发达国家市场成熟,发展中国家需求增长快。
-
与现有传统产品的对比及替代潜力:
- 主要竞品/传统方案:自体皮移植、异体皮、脱细胞异体/异种真皮 (ADM)、合成敷料、其他生物敷料 (如壳聚糖、海藻酸盐、透明质酸基材料)。
- 本材料产品的核心优势:优异的生物相容性和低免疫原性,引导真皮再生和上皮化,减少疤痕形成和挛缩,良好的液体管理和屏障功能。
- 预期市场替代潜力评估:高。有望替代部分ADM和传统生物敷料,并在某些情况下减少对自体皮的需求。
- 替代可行性分析:临床需证明其愈合速度、愈合质量(疤痕、弹性、外观)、感染控制及成本效益。
- 本材料在该产品的年度商业价值潜力估算:若能占据皮肤替代品市场10-20%的份额,则年度商业价值可达2.5亿至7亿美元。
产品/产品类别:骨修复材料 (Bone Graft Substitutes / Bone Repair Materials)
- 核心功能与应用场景:用于填充骨缺损、促进骨折愈合、脊柱融合、牙槽骨增量等。提供成骨的支架 (osteoconduction)、诱导骨形成 (osteoinduction) 或含有成骨细胞 (osteogenesis)。
- 适用材料形态:颗粒、块状、可塑性腻子、多孔支架 (海绵状、3D打印)、膜 (用于引导骨再生GBR)。
- 目标临床应用领域:骨科、口腔种植科、颌面外科、神经外科 (脊柱融合)。
-
全球市场规模评估 (年度):
- 当前市场总值:全球骨移植和替代物市场规模约为30-40亿美元 (数据年份:2023-2024年,行业估算)。胶原蛋白是天然骨组织的主要有机成分,广泛应用于人工骨组织工程材料 (中国组织工程研究)。
- 估算方法/数据来源:行业综合估算。
- 主要区域市场分布 (年度):北美、欧洲市场份额高,亚太地区因人口老龄化和医疗水平提升,增长潜力大。
-
与现有传统产品的对比及替代潜力:
- 主要竞品/传统方案:自体骨 (金标准但来源有限、额外创伤)、同种异体骨 (有免疫和疾病传播风险)、异种骨、合成材料 (如磷酸钙陶瓷TCP/HA、生物活性玻璃、硫酸钙)、脱矿骨基质 (DBM)。
- 本材料产品的核心优势:良好的骨引导性和骨整合能力,可作为生长因子/药物载体,可控的降解速率,优异的生物相容性和低免疫原性,可塑性和可加工性。
- 预期市场替代潜力评估:中到高。特别是在与成骨活性物质(如BMPs)复合后,或与磷酸钙等无机成分复合形成仿生骨材料,有望替代部分自体骨、同种异体骨和现有合成骨替代物。
- 替代可行性分析:需证明其成骨效果、力学支撑能力(尤其在承重部位)、降解特性和安全性。
- 本材料在该产品的年度商业价值潜力估算:若能占据骨修复材料市场5-15%的份额,则年度商业价值可达1.5亿至6亿美元。
市场价值评估注意事项
上述市场规模和商业价值潜力估算均为初步分析,实际数值会受到多种因素影响,包括:
- 最终产品的临床试验结果和获批适应症范围。
- 生产成本和最终市场定价策略。
- 各国医疗器械监管审批的进度和要求。
- 医保覆盖情况和支付意愿。
- 市场推广和医生接受程度。
- 竞争对手的策略和新技术的出现。
因此,在制定商业计划时,需要进行更深入、更细致的市场调研和财务分析。
市场价值总览与战略展望
基于前述对重点植入类产品的市场分析,我们可以对高强度可溶性胶原蛋白医学再生材料的整体市场潜力进行概览,并探讨其商业化的关键成功因素与面临的挑战。
1. 综合市场价值排序与概览
下表汇总了部分重点产品类别的预估全球年市场总值及其在高强度胶原蛋白材料应用下的潜力。请注意,这些数值是基于当前市场状况和材料特性进行的估算,实际市场表现会因多种因素而异。
| 排名 | 产品/产品类别 | 预估全球年市场总值 (亿美元,2023-2024年估) | 核心应用领域 | 主要材料形态 | 本材料替代潜力 (简评) | 本材料预估年商业价值潜力 (亿美元) |
|---|---|---|---|---|---|---|
| 1 | 疝修补片 | 50-70 | 普外科、腹壁修复 | 膜/片状、编织型 | 高 (替代部分合成及现有生物补片) | 5 - 14 |
| 2 | 可吸收手术缝线 | 40-60 | 通用外科、多科室 | 线型 | 高 (尤其高端市场) | 2 - 9 |
| 3 | 皮肤修复膜/人工真皮 | 25-35 | 烧伤科、创面修复 | 膜/片状 | 高 (替代部分ADM及传统敷料) | 2.5 - 7 |
| 4 | 骨修复材料 | 30-40 | 骨科、口腔科 | 多形态 (颗粒、膜、支架等) | 中到高 (尤其复合型材料) | 1.5 - 6 |
| 5 | 人工神经导管 | 3-5 | 神经外科、手外科 | 管型 | 高 (替代部分自体移植及现有导管) | 0.45 - 1.5 |
| 注:上表数据为行业估算,仅供参考。其他潜在产品如心包补片、口腔修复膜、硬脑膜补片、小口径人工血管等,其市场规模需进一步专项调研,但同样具有可观的商业前景。 | ||||||
2. 高强度胶原蛋白材料整体市场应用前景总结
高强度可溶性胶原蛋白医学再生材料凭借其独特的生物学特性组合——即高强度、卓越的生物相容性、极低的免疫原性、可控的生物降解性、强大的组织修复与再生促进能力,以及优异的可加工性——在众多植入类医疗器械领域展现出替代传统材料并开拓全新应用的巨大潜力。该材料不仅有望提升现有治疗手段的疗效和安全性,更有可能催生全新的治疗方案,特别是在组织工程和再生医学领域。
总体而言,该材料的市场前景广阔,有望成为下一代医学再生材料的平台型技术。其核心价值主要体现在以下三大方向:
- 创伤修复:如皮肤缺损、软组织损伤的快速、高质量愈合。
- 组织重建:如疝修补、硬脑膜修复、骨缺损填充等,恢复组织结构的完整性。
- 再生医学:如神经再生、肌腱/韧带再生、血管再生等,实现组织功能的根本性恢复。
随着技术的成熟和临床应用的拓展,预计该材料将在全球医用植入物市场中占据越来越重要的份额。
3. 商业化关键成功因素与挑战
要将这一创新材料成功推向市场并实现其商业价值,需要关注以下关键成功因素并应对相关挑战:
关键成功因素:
- 确凿的临床证据:大规模、多中心、高质量的随机对照临床试验是证明产品安全性和有效性的金标准,也是获得医生和患者信任、进入临床指南和医保目录的基础。
- 稳定的规模化生产工艺与质量控制:建立符合GMP(药品生产质量管理规范)要求的生产线,确保产品批次间性能的一致性和高品质,是商业化的前提。
- 清晰的法规审批路径与高效执行:深入理解并遵循各国(尤其是目标市场如美国FDA、欧盟CE、中国NMPA)医疗器械注册法规,制定合理的注册策略,高效推进审批流程。重组胶原蛋白生物材料已有命名指导原则和审查指导原则可供参考 (国家药监局指导原则, CMDE审查指导原则)。
- 成本效益优势:在保证卓越性能的前提下,通过工艺优化和规模化生产,实现具有竞争力的价格。或者,通过减少并发症、缩短住院时间、降低二次手术率等方式,体现其在整体医疗经济学上的价值。
- 有效的市场教育与学术推广:通过学术会议、专业培训、发表高质量研究论文等方式,提升临床医生对新材料特性、优势和临床价值的认知和接受度。
- 强大的知识产权保护:通过专利布局,构筑技术壁垒,保护核心创新,确保市场竞争优势。
面临的挑战:
- 从实验室到产业化的放大效应:在实现大规模生产的过程中,如何保持材料在实验室阶段所展现的优异特性,并有效控制成本,是一个重要的工程技术挑战。重组胶原蛋白的规模化生产依赖生物工程技术,工艺复杂 (2024重组胶原蛋白行业白皮书)。
- 长期体内安全性和有效性的验证:对于植入类医疗器械,尤其是可降解吸收的再生材料,其长期的体内安全性和有效性(如降解产物的安全性、远期组织再生效果的稳定性)需要更长时间的临床随访数据来证实。
- 与成熟市场领导者的竞争:现有医用植入物市场,特别是一些大宗产品(如缝线、疝补片),已被少数跨国巨头主导,新进入者面临激烈的市场竞争。
- 医保支付和定价策略:如何使创新产品获得合理的医保支付价格,并被纳入各国的医保报销目录,是影响市场推广速度和规模的关键因素。
- 复杂组织/器官再生的技术瓶颈:对于结构和功能更为复杂的组织或器官(如人工血管、人工肠道等),尽管高强度胶原蛋白材料提供了理想的基材,但实现其完全的功能性再生仍面临细胞来源、血管化、神经支配、免疫调控等多方面的科学和工程技术瓶颈。
结论:把握先机,引领医学再生材料创新浪潮
高强度可溶性胶原蛋白医学再生材料的研发成功,标志着在生物医用材料领域取得的一项重要突破。其独特的性能组合使其在众多临床应用中展现出取代传统材料并开创全新治疗模式的巨大潜力。
1. 最具商业化潜力的重点产品方向 (Top 3-5)
综合市场需求、技术成熟度以及本材料的特性优势,以下产品方向被认为具有最高的近期商业化潜力:
- 可吸收手术缝线:市场需求基数庞大,本材料在低炎症、微疤痕、促愈合方面的优势直击临床痛点,尤其在高端市场(整形、精细外科、儿童外科)有望快速渗透。
- 疝修补片与皮肤修复膜/人工真皮:这两类产品临床用量大,市场对生物相容性和组织再生效果的要求日益提高。本材料有望提供更优的解决方案,替代部分现有合成材料和生物材料,市场空间广阔。
- 人工神经导管:解决周围神经缺损修复这一临床难题,技术壁垒相对较高,产品附加值也高。用户团队已有的动物实验成功案例为此方向奠定了坚实基础。
- 骨修复材料(特别是复合型):骨缺损修复市场需求稳定增长,本材料作为优良的生物支架,与成骨活性因子或无机骨成分复合,有望开发出性能卓越的新一代骨修复产品。
2. 核心价值主张的再强化
高强度可溶性胶原蛋白医学再生材料的核心价值主张可以凝练为:“一种兼具卓越力学性能与极致生物活性的革命性医学再生材料平台,致力于通过促进高质量的组织修复与功能重建,为全球患者提供更安全、更有效、更符合生理需求的创新医疗解决方案。”
3. 下一步行动框架/考虑要点 (战略层面建议)
为成功将这一创新技术转化为具有市场竞争力的产品,并抓住历史机遇,建议贵团队考虑以下战略层面要点:
- 聚焦与突破:在众多潜在产品中,优先选择1-2个最具市场潜力且技术转化路径相对清晰的产品方向(如上述Top 3-5中的部分产品),集中研发、临床和注册资源,力求率先取得市场突破,树立品牌标杆。
- 临床研究驱动:精心设计并严格执行高标准的多中心随机对照临床试验(RCT),获取充分、可靠的临床数据,不仅用以支持产品注册,更要为市场推广和学术认可提供强有力的循证医学证据。
- 工艺优化与成本控制:持续投入研发,优化高强度胶原蛋白材料的规模化生产工艺,在保证质量的前提下努力降低生产成本,以提升产品的市场竞争力及可及性。
- 全球化视野与本土化策略:从早期即规划全球市场布局,针对不同国家和地区的法规要求、市场特点、医疗水平和支付能力,制定差异化的市场准入和推广策略。
- 生态系统构建:积极寻求与国内外顶尖的科研机构、临床医学中心、产业资本、以及有经验的医疗器械营销渠道伙伴建立战略合作关系,共同推进技术创新、临床转化和市场拓展,构建协同发展的创新生态系统。
- 持续创新与迭代:在第一代产品成功上市的基础上,保持研发投入,不断探索材料的进一步改性(如表面功能化、负载特定生物活性分子)、与其他材料的复合应用(如与陶瓷、其他生物聚合物复合)、以及结合3D生物打印等前沿制造技术,拓展新的适应症和开发更高端的第二代、第三代产品。
结语:
展望未来,高强度可溶性胶原蛋白医学再生材料凭借其在力学性能、生物相容性、可降解性及促再生能力等方面的多项突破性优势,有望在外科、骨科、神经科、皮肤科、口腔科乃至心血管等众多医疗领域引发深刻变革。这不仅能为全球数以百万计的患者带来更优的治疗选择和显著改善的生活质量,也将为贵研究团队带来巨大的商业成功和社会价值。把握这一历史性的发展机遇,坚持科学严谨的态度,勇于开拓创新,必将在医学再生材料的创新浪潮中书写新的传奇篇章。
本材料的潜力:通过构建具有仿生多层结构(模拟食管黏膜层、黏膜下层、肌层)的管状胶原支架,并可选择性负载促进上皮细胞和肌细胞再生的生长因子,有望引导宿主细胞原位再生出具有正常蠕动功能和屏障功能的食管组织。这种“原位再生”的人工食管,理论上能更好地恢复食管的生理功能,减少并发症。
预期效益:为食管缺损患者提供一种创伤更小、并发症更少、术后生活质量更高、更接近生理状态的食管重建新方案,显著改善患者的营养状况和生存尊严。
市场规模预估:食管癌发病率较高,对高质量食管重建技术的需求持续存在。该领域的技术突破将带来巨大的临床价值。
其他极具潜力的应用方向 (简要提及):
- 全层皮肤替代物:用于大面积深度烧伤、慢性难愈合创面(如糖尿病足溃疡、压疮)的修复,促进真皮和表皮同步再生,减少瘢痕挛缩。
- 硬脑(脊)膜修复补片:用于神经外科手术后硬脑(脊)膜缺损的修补,有效预防脑脊液漏,促进硬膜再生。
- 膀胱组织工程化修复:用于膀胱部分切除术后或神经源性膀胱等功能障碍性疾病的修复,重建具有储尿和排尿功能的膀胱壁。
- 心肌补片/心脏瓣膜组织工程:用于心肌梗死后坏死心肌的修复,或作为构建组织工程心脏瓣膜的基质材料,应对心力衰竭和瓣膜性心脏病。
- 软骨组织工程:用于关节软骨损伤(如骨关节炎、运动损伤)的修复,促进透明软骨再生,恢复关节功能。
市场潜力综合分析与价值展望 - 描绘商业成功的宏伟蓝图
本可溶性胶原蛋白基仿生再生材料技术平台,凭借其在多种关键软组织修复领域的突破性表现和广泛的可拓展性,展现出巨大的市场潜力。根据行业报告(如 Grand View Research, MarketsandMarkets 等),全球再生医学市场规模预计在未来十年将保持高速增长,到2030年有望达到或超过500亿至数千亿美元的量级,年复合增长率(CAGR)预计在15-25%之间。我们的技术直接切入其中多个高价值、高增长的细分市场:
我们的技术作为一种可能从根本上改变现有治疗范式的颠覆性创新,有望在上述各领域获得可观的市场份额。除了巨大的商业价值外,本技术的成功应用还将带来显著的社会经济效益:通过提供更有效、更安全的治疗方案,可以显著改善患者的生活质量,缩短康复周期,减少并发症和再次手术的发生率,从而降低整体医疗成本,减轻社会医疗负担。
关键要点总结
本仿生再生材料不仅在已验证的肌腱、肌肉、神经和缝线应用中展现出深化潜力,更有望拓展至人工血管、气管、食管等多个高需求、高价值的全新领域。其作为平台型技术的广泛适用性,预示着巨大的市场容量和深远的社会经济价值,是再生医学领域一个极具吸引力的投资和合作标的。
